近期,我校第二附属医院陶辉副教授、张野教授与上海交通大学医学院附属新华医院的赵健元教授,在心血管领域权威期刊《欧洲心脏杂志(European Heart Journal)》(IF=38.1)上发表题为《SLC31A1缺失导致线粒体铜耗竭并促进心肌纤维化(SLC31A1 loss depletes mitochondrial copper and promotes cardiac fibrosis)》的原创性研究论文。第二附属医院研究生涂彬、宋凯和上海交通大学医学院博士后周泽宇为论文的第一作者,陶辉、张野和赵健元为共同通讯作者,我校为第一完成单位和最后通讯作者单位。
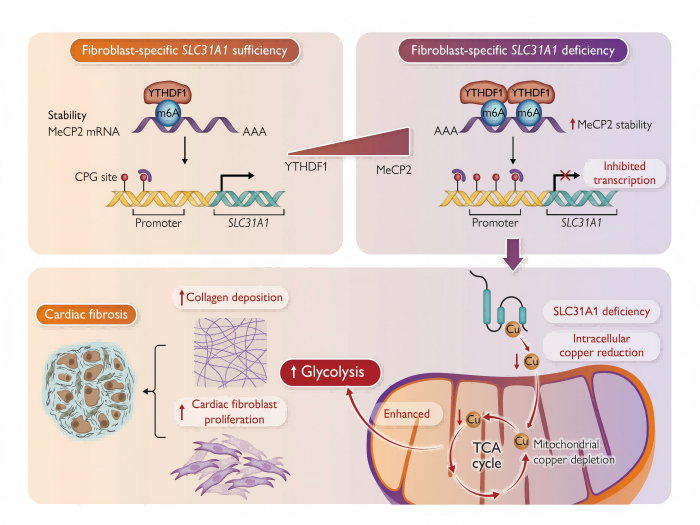
研究发现一种新的表观遗传机制。该机制通过调控铜转运分子SLC31A1的表达,诱导线粒体铜离子耗竭,铜耗竭导致氧化磷酸化受损,进而刺激糖酵解的发生,最终激活心肌成纤维细胞并促进心肌纤维化。这一发现为心肌纤维化的预防策略开发提供了新方向。
《欧洲心脏杂志》同期刊发了由德国法兰克福大学心血管研究中心、心血管再生研究所研究组长,卓越集群“心肺研究所”下属机构CPI学院发言人朱利安·瓦格纳(Julian U.G. Wagner)教授的述评 “铜与心肌纤维化:疾病与健康的微妙平衡”。朱利安·瓦格纳教授表示,这项研究首次系统阐明了铜代谢动态如何通过表观遗传机制驱动心肌纤维化。未来,通过调节SLC31A1或铜离子稳态,可能开发出抑制纤维化、改善心功能的新疗法。研究还提示了SLC31A1在心肌梗死不同阶段的表达差异可能成为疾病分期的生物标志物,结合患者个体化表观遗传特征,未来或可实现心肌纤维化的精准干预。
此外,陶辉、赵健元合作研究还发现,钙离子异常增高会致使自噬异常,引发心肌成纤维细胞活化。而抑制钙离子摄入,能够有效遏制成纤维细胞的迁移与活化。题为《YTHDF1 依赖性PIEZO2 mRNA m6A修饰对心肌纤维化的表观转录调控(Epitranscriptomic regulation of cardiac fibrosis via YTHDF1-dependent PIEZO2 mRNA m6A modification)》的相关原创性研究成果,发表于《心血管研究(Cardiovascular Research)》(IF=10.4)。杂志同期刊发了由意大利心血管病专家毛里齐奥·佩斯(Maurizio Pesce) 教授的述评“当细胞力学遇到表观转录组学:减少Piezo2 RNA中m6A修饰可改善心肌纤维化”。

这一系列发现,揭示了金属离子这一常被忽视的因素在心肌纤维化进程中的作用,不仅加深了学界对心肌纤维化机制的理解,也为突破现有治疗瓶颈、开辟全新治疗路径提供了理论依据 。(第二附属医院 科技产业部)
论文链接:
《SLC31A1 loss depletes mitochondrial copper and promotes cardiac fibrosis》: https://doi.org/10.1093/eurheartj/ehaf130
《Epitranscriptomic regulation of cardiac fibrosis via YTHDF1-dependent PIEZO2 mRNA m6A modification》:https://doi.org/10.1093/cvr/cvae239

