5月4日,我校曹云霞教授团队联合清华大学医学院那洁副教授团队和首都医科大学李琳博士,在生物医学领域著名期刊《蛋白质与细胞(Protein & Cell)》(IF=10.164)在线发表题为《母源性CHEK1基因杂合突变导致受精卵卵裂障碍(Maternal heterozygous mutation in CHEK1 leads to mitotic arrest in human zygotes)》的论文。该研究是曹云霞教授团队的又一重要成果,阐述了受精卵第一次卵裂障碍的致病基因CHEK1突变及其引起女性不孕的机制,不仅为该类疾病的研究提供了新的理论依据,也为因CHEK1蛋白活性失调造成的不孕症提供了潜在解决方案。
不孕不育影响着全球12%-15%的育龄期夫妇,即使体外受精技术(IVF/ICSI)的快速发展,仍有相当比例的不孕夫妇无法实现成功孕育子代的愿望。尤其是经历了数个周期的助孕治疗均未获得理想的胚胎可供移植,给患者带来了沉重的精神打击和经济压力,而这类情况的出现多与遗传因素相关。正常妊娠的建立需要配子的成熟、受精及早期胚胎的发育。成熟卵子和精子结合形成受精卵后开始进入第一次有丝分裂,此过程发生障碍会导致胚胎早期发育的失败。
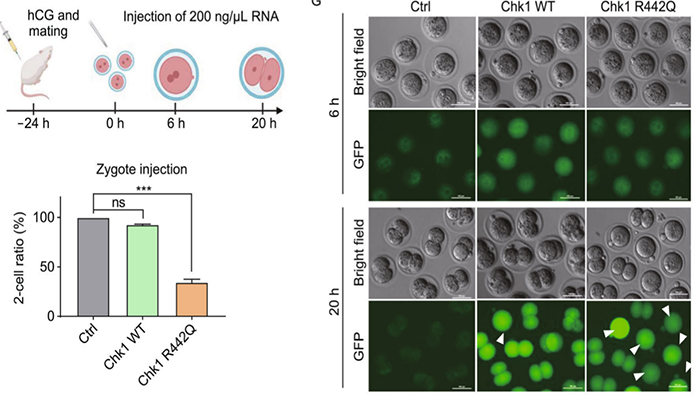
该研究从临床入手,通过对一例表现为受精卵卵裂失败的女性不孕家系进行全外显子测序及高效的生物信息学分析,发现了潜在的致病突变CHEK1 R442Q。作为DNA损伤检查点激酶,当细胞中发生DNA损伤时,CHEK1激酶活化,阻止细胞周期向下进行并启动修复程序,直到DNA错误修复或细胞凋亡。研究人员克隆了对应的小鼠Chk1突变mRNA,并通过显微注射的手段将其引入小鼠受精卵,突变的Chk1蛋白同样造成了半数以上小鼠受精卵第一次有丝分裂的阻滞。体外纯化的蛋白激酶活性实验表明,此突变显著提高了CHEK1激酶活性。升高的CHEK1激酶活性使得第一个有丝分裂检查点阈值过高,在不存在DNA损伤或错误的情况下,细胞周期依然无法向下进行。
为寻找此突变造成的不孕症的解决方案,研究团队进一步利用CHEK1的抑制剂处理了引入了突变Chk1蛋白的小鼠的受精卵,经处理的受精卵进一步发育的比例大大提升,并可以在移植后出生健康的子代。研究还表明,低剂量的CHEK1抑制剂处理没有造成更多的DNA损伤,也并未造成显著的转录组改变。该研究揭示了人类早期胚胎第一次有丝分裂对DNA损伤检查点调控极其敏感,并提供了因CHEK1蛋白活性失调造成的不孕症的潜在解决方案。

我校第一附属医院为文章第一作者单位,该院陈蓓丽博士及清华大学医学院博士后郭健颖、博士生王婷为本论文共同第一作者。曹云霞教授、章志国副教授以及清华大学那洁副教授、首都医科大学附属北京妇产医院助理研究员李琳博士为该论文共同通讯作者。
本研究报道了因CHEK1基因错义突变导致的女性不孕家系。CHEK1 R442Q位点的突变造成了CHEK1激酶活性增强,进而阻滞了受精卵的第一次有丝分裂。利用低剂量CHEK1 抑制剂对阻滞的受精卵短时间处理,显著恢复了突变造成的阻滞作用,使受精卵顺利发育并产生健康子代。该研究解释了因CHEK1突变造成的女性不孕机制并寻找到了潜在的治疗方法,为此类特殊病人的不育症治疗提供了新思路。研究团队后期将致力于本研究成果在临床治疗上的进一步探索,以达到真正帮助患者的目的。(第一附属医院 丁方方)
原文链接:https://link.springer.com/article/10.1007/s13238-021-00844-9

